3月31日,中国科学院上海营养与健康研究所应浩研究组在Journal of Molecular Cell Biology期刊在线发表了题为“NAD+ subcellular partitioning mediated by miR-183 and miR-96 regulates muscle stem cell differentiation”的研究论文。该研究揭示了关键调控因子miR-183和miR-96通过调控代谢辅因子NAD+亚细胞分布,进而调控骨骼肌干细胞分化和骨骼肌再生的分子机制,为骨骼肌损伤修复、肌肉相关疾病的干预提供了新的理论依据和潜在靶点。
骨骼肌再生是一个复杂的动态调控过程,依赖于骨骼肌干细胞(MuSC)的精准平衡——损伤后被激活、增殖以提供足够细胞量,适时分化为成熟肌纤维完成修复,同时保留部分干细胞用于自我更新,为后续再生储备资源。一旦这一平衡被打破,可能导致骨骼肌再生失败或相关病理状态的发生。NAD+作为细胞内关键的代谢辅因子,对骨骼肌干细胞功能具有重要调控作用,但NAD+的空间分布如何影响骨骼肌干细胞功能,其调控机制一直尚不明确。
研究团队通过一系列体内外实验发现,miR-183和miR-96在骨骼肌前体细胞中高表达,且在损伤后的再生肌肉中显著上调。miR-183和miR-96的双敲除小鼠,骨骼肌损伤后再生效率显著下降,骨骼肌干细胞出现过早分化,导致干细胞库耗竭,反复损伤后再生缺陷进一步加剧。
进一步机制研究发现,miR-183和miR-96通过直接靶向线粒体NAD+转运蛋白SLC25A51,调控NAD+的亚细胞分布。当miR-183和miR-96缺失时,SLC25A51表达升高,导致线粒体NAD+水平增加,而胞质NAD+水平降低。这种NAD+的亚细胞分布异常,通过两条路径共同调控骨骼肌干细胞分化:一方面,胞质NAD+减少会削弱SIRT1介导的去乙酰化作用,导致肌源性基因启动子区H4K16ac水平升高,促进分化基因表达;另一方面,线粒体NAD+积累会激活三羧酸循环,升高腺嘌呤核苷三磷酸(ATP)和柠檬酸水平,这些代谢物通过变构激活ACLY通路,增加乙酰辅酶A生成,为H4K16ac提供乙酰基团,进一步推动分化。研究还发现,线粒体中主要的NAD+依赖型去乙酰化酶SIRT3在miR-183/96缺失细胞中活性显著升高,SIRT3敲低会损害成肌分化,并削弱miR-183/96缺失细胞中ATP和乙酰辅酶A的升高,表明线粒体NAD+还可以通过SIRT3参与骨骼肌干细胞分化的调控过程。
该研究首次将miRNA、NAD+亚细胞分布与骨骼肌干细胞命运调控相结合,建立了miR-183/96-SLC25A51-NAD+-SIRTs的调控轴,揭示了代谢重编程与表观遗传修饰协同调控骨骼肌干细胞命运的新机制,明确了miR-183和miR-96作为骨骼肌干细胞分化时序的关键调控因子,为骨骼肌损伤修复、肌营养不良等疾病的治疗提供了新的靶点和思路。
此次在线发表的研究,是研究团队围绕miR-183簇开展的系列研究的重要延伸。miR-183簇包含miR-183、miR-96和miR-182三个microRNA,因三者种子序列高度同源而归为同一家族,研究团队此前针对该簇的系列研究已逐步揭示其在骨骼肌代谢调控中的关键作用:miR‑182通过靶向FoxO1/PDK4调控骨骼肌葡萄糖利用,维持全身糖代谢稳态;而miR‑183/96可同时靶向FoxO1/PDK4与ATGL,一方面促进葡萄糖氧化利用,另一方面抑制肌内脂解与脂肪酸氧化,实现对葡萄糖与脂肪两种能量底物利用的双向协调,精细重塑骨骼肌燃料选择与代谢稳态。
综上,研究团队通过系列研究,系统阐明了miR-183簇(miR-183、miR-96及miR-182)在骨骼肌生理功能调控中的核心作用,构建了“miR-183簇—靶蛋白—代谢通路/表观遗传调控”的完整分子网络:从最初发现其对骨骼肌糖脂代谢和能量稳态的调控,到最新揭示其通过NAD⁺亚细胞分区调控骨骼肌干细胞分化与骨骼肌再生,逐步完善了对miR-183簇生物学功能的认知。这些研究成果不仅深化了对microRNA调控骨骼肌代谢与再生机制的理解,也为骨骼肌损伤修复、肌萎缩、肥胖及糖尿病等代谢相关疾病的干预提供了新的分子靶点和理论基础。
营养与健康所博士毕业生马梅、博士研究生马睿森为该论文的共同第一作者,应浩研究员和李俞莹副研究员为共同通讯作者。该研究得到了科技部、国家自然科学基金委员会、中国科学院空间应用工程与技术中心,以及上海市等项目的资助。
论文链接:
https://academic.oup.com/jmcb/advance-article/doi/10.1093/jmcb/mjag015/8566319
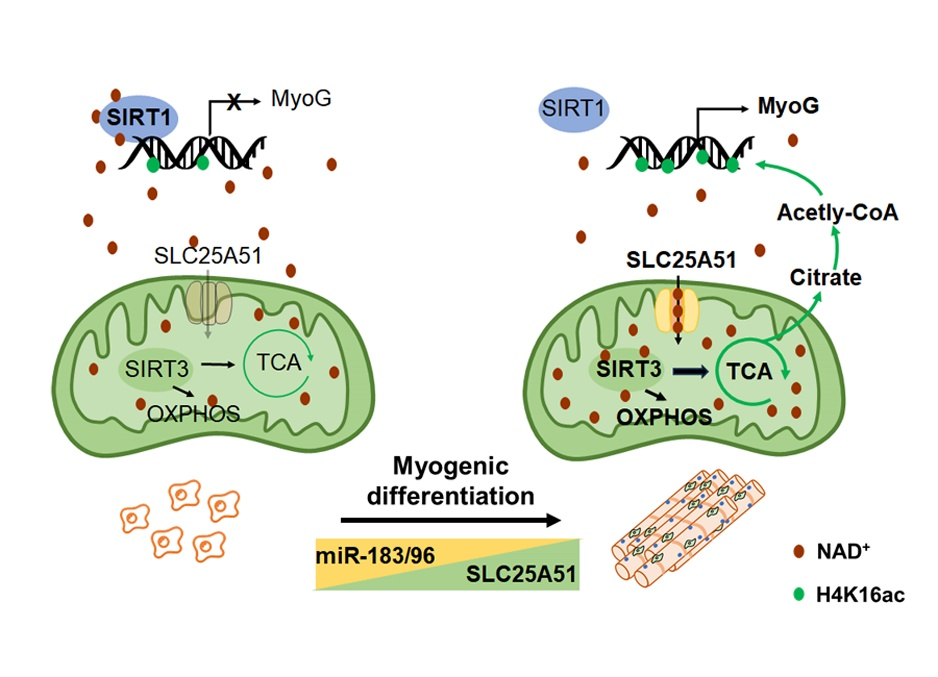
图:miR-183和miR-96通过调控NAD+亚细胞分布,进而调控骨骼肌干细胞分化和骨骼肌再生分子机制图
推送单元:应浩研究组、科技规划与任务处