4月7日,中国科学院上海营养与健康研究所章海兵研究组在国际学术期刊《美国国家科学院院刊》(PNAS)在线发表了题为“RIPK1 ubiquitination regulates its kinase independent function in development and inflammation”的研究成果。该研究聚焦RIPK1关键泛素化位点K376的功能,通过构建多种遗传小鼠模型,系统解析了RIPK1通过泛素化修饰在个体发育和炎症调控中的双重作用,为RIPK1相关炎症性疾病的发病机制研究和干预策略提供了重要理论框架。
系统性自身炎症性疾病(Systemic Autoinflammatory Diseases, SAIDs)是由先天免疫系统异常激活引发的一类疾病。近年来,基础和临床研究表明,程序性细胞死亡通路相关基因突变在其发病中起核心作用。然而,程序性细胞死亡与炎症反应之间的互作机制,仍是该领域亟待破解的关键科学问题。
RIPK1作为调控细胞死亡和炎症反应的核心枢纽分子,其功能受多种翻译后修饰精细调控。其中,K376位点的泛素化已被证实能有效抑制细胞凋亡和坏死性凋亡,但在炎症调控中的具体作用机制此前尚不清晰。人类遗传学研究显示,RIPK1功能异常与自身炎症性疾病密切相关:RIPK1缺失可导致免疫缺陷,剪切位点突变引发自身炎症综合征,而近期发现的RIPK1泛素化缺陷突变(K377E/R390G)进一步提示,泛素化异常与系统性炎症之间存在直接关联。因此,深入解析RIPK1泛素化在炎症中的作用,对阐明SAIDs发生发展机制并探索精准干预策略具有重要意义。
章海兵研究组长期致力于程序性细胞死亡及其在炎症调控中的机制研究。前期工作通过构建Ripk1K376R突变小鼠模型,阐明了RIPK1 K376位点泛素化通过抑制细胞凋亡和程序性坏死,在维持个体发育中发挥关键作用(Nat Commun.2019.PMID: 31519886)。在此基础上,该研究进一步构建了Ripk1K376R/D138N等双点突变小鼠模型,发现K376位点泛素化缺失会导致RIPK1异常激活:在胚胎期通过激酶依赖性途径诱导过度细胞死亡,引发胚胎致死;而在引入激酶失活突变(D138N)后,虽能挽救胚胎致死,但小鼠仍表现出进行性系统性炎症,包括皮肤和肝脏炎症、脾脏肿大以及免疫稳态失调。
机制研究进一步揭示,RIPK1 K376R突变不仅影响其激酶活性,还通过支架功能驱动炎症反应。具体而言,该突变可激活内源性NLRP3炎症小体,促进IL-1β分泌。遗传学证据显示,Caspase-1/11缺失能显著缓解炎症,而TRIF缺失则无明显作用,明确了炎症小体通路的核心地位。此外,分析证实这一炎症过程不依赖于MLKL介导的程序性坏死,而是主要依赖RIPK3及Caspase-1/11介导的炎症小体通路,从而揭示了一种非经典的炎症调控机制。
综上,该研究系统阐明了RIPK1泛素化在细胞死亡与炎症调控中的关键作用,揭示了RIPK1通过泛素化修饰抑制“激酶依赖性细胞死亡与激酶非依赖性炎症”双重稳态调控新机制,为“程序性细胞死亡与炎症反应的互作机制”这一重要科学问题提供了重要证据支撑,同时为SAIDs的精准诊断和靶向治疗提供了新思路与潜在干预靶点,为临床转化奠定了理论基础。
中国科学院上海营养与健康研究所副研究员李明,博士研究生刘建玲、邢铭烟、刘涵为该论文的共同第一作者。中国科学院上海营养与健康研究所章海兵研究员和李明副研究员为该论文共同通讯作者。该研究工作得到了中国科学院上海营养与健康研究所李于研究员、李虹研究员的大力支持。该研究受科技部国家重点研发计划、国家自然科学基金及上海市重大研究计划等项目资助,并依托中国科学院上海营养与健康研究所所级公共技术中心分析测试技术平台与实验动物技术平台完成。
原文链接:https://www.pnas.org/doi/10.1073/pnas.2520356123
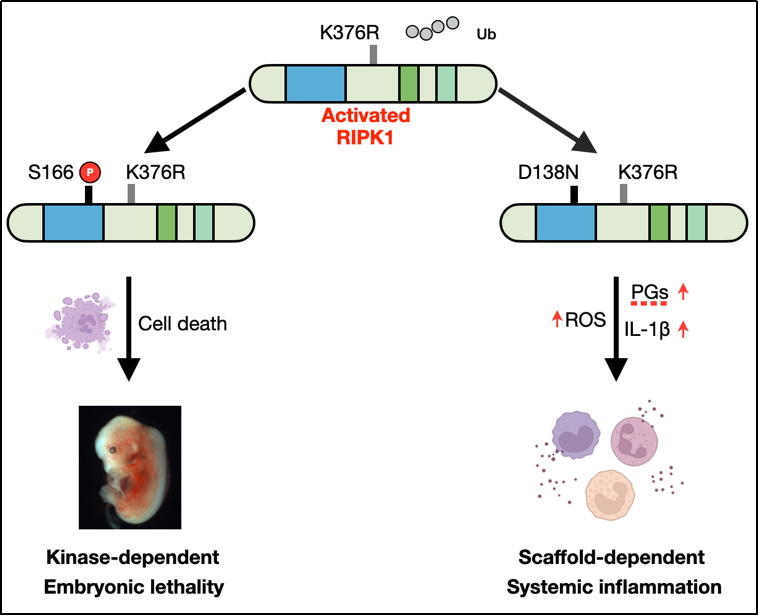
图:RIPK1泛素化修饰调控激酶依赖性细胞死亡与激酶非依赖性炎症示意图
推送单元:章海兵研究组、科技规划与任务处